水的pH值(酸碱度)是水质的重要指标,若水体pH值超出 6.5~8.5,水体中微生物生长会受到一定程度的抑制,
影响水体的自净能力;若水体长期受到酸、碱污染,将对生态平衡产生不良影响。 因而pH值是环境监测工作中水体的一项必
测项目。 但在实际工作中,部分实验室出现一些做不准的现象,笔者针对实验室常出现的问题作出总结,并提出解决方案。
PH计测定原理:
目前大多数实验室pH计原理是采用电位分析测法测量溶液pH值,仪器是由参比电极、指示电极及精电位计三部分组成.
通过将玻璃电极(指示电极)和汞电极(参比电极)插入被测溶液中,组成一个电化学电池,化学能转变成电能,其中参比电
位在一定温度下是定值,指示电极电位随 pH 值变化而变化。
牢记校准过程温补偿
温度是影响 pH 值测量结果很重要的因素,仪器标 准 溶 液 校 准 操 作 程 序 按 说 明 书 操作。须注意调节仪器的补偿装
置与溶液的温度一致,并使被测样品与校正仪器用的标准缓冲溶液温度误差在± 1℃ 之内。 一般先将待测与准溶液放在室温,
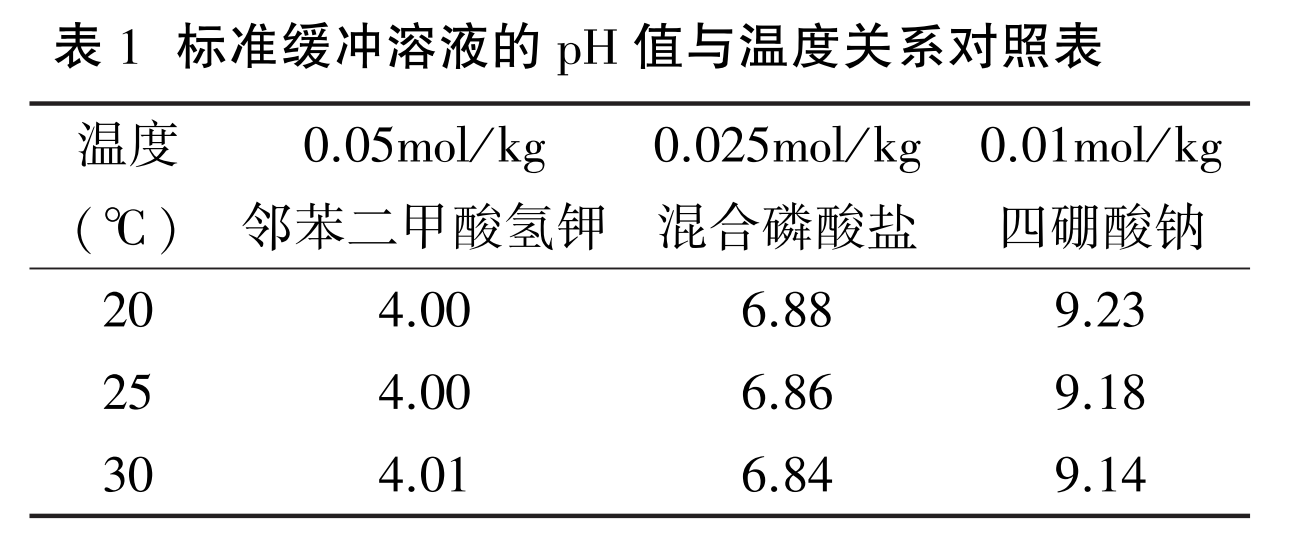
待溶液温度稳定,使用温 度测量出室温下溶液的温度,并将仪器温度补偿旋钮调至该温度。 常用缓冲溶液和温度的关系,见表
( 一般按照 25℃ 下缓冲溶液 pH 值标定) 。